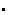- GlucoSober®二氢小檗碱,独特晶型专利工艺
- 2024年07月12日来源:中国网
提要:随着全球经济的发展和生活方式的改变,肥胖、高血糖和高血脂已经成为威胁人类健康的三大主要问题。这些问题不仅影响个人的健康和生活质量,还对社会和经济产生了巨大的负担。
本文首发自微信公众号德诺邦尚,我已委托“维权骑士”为我的文章进行维权行动。
随着全球经济的发展和生活方式的改变,肥胖、高血糖和高血脂已经成为威胁人类健康的三大主要问题。这些问题不仅影响个人的健康和生活质量,还对社会和经济产生了巨大的负担。而随着有减肥或血糖控制需求的人群开始关注具有血糖调节功能的天然活性成分时,小檗碱因其具有多种生物活性,并具有不错的血糖调节和脂肪调节活性而受到人们的青睐。
从2022年下半年开始,小檗碱在美国版抖音—TikTok上爆红,起因是某消费者在TikTok上记录了使用小檗碱减肥成功的经历,收到了广泛的传播和讨论,以及效仿。美国消费者称小檗碱为“天然的Ozempic(司美格鲁肽)”,用小檗碱减肥相关的视频在短时间内就达到了累计上亿的播放量。这一社交媒体现象促使欧美市场小檗碱产品热卖,多家品牌商表示小檗碱产品均卖断货,甚至一度造成小檗碱的原料紧缺。
小檗碱,天然GLP-1,多重健康机制
小檗碱,又称“黄连素”,具有悠久的使用历史。在中国最早见于3000多年前的《神农本草经》,在印度的《阿育吠陀》药典中也可见小檗碱的使用记载。小檗碱最初主要用于抗菌和抗病毒、以及止泻等。近年来,随着现代科学的发展,小檗碱的多种药理作用逐渐被揭示,并广泛应用于临床实践中。研究发现,小檗碱主要通过以下机制发挥健康效益。
01促进GLP-1分泌
通过促进胰高血糖素mRNA的表达与肠道L-细胞的增殖,增加GLP-1的分泌。[1]
通过激活在肠道中表达的苦味受体TAS2R38,刺激肠道L-细胞分泌GLP-1。[1]
02调节血糖代谢,改善胰岛素抵抗
刺激胰岛素受体的表达,增强胰岛素敏感性,改善胰岛素抵抗。[2]
上调葡萄糖转运体Glut 4的表达,促进细胞吸收葡萄糖,从而降低血液中的葡萄糖水平。[3]
减少线粒体中氧气的消耗和ATP的产生,抑制葡萄糖异生转录因子(G6Pase和PEPCK)的表达,抑制肝脏葡萄糖异生成,降低空腹血糖水平。[4]
03增加棕色脂肪含量,改善脂肪代谢
促进白色脂肪组织中与棕化基因的表达,增加棕色脂肪的数量,并能增强棕色组织的功能,促进能量消耗和产热。[5]
通过AMPKα抑制与脂肪生成基因相关的转录子SREBPs和ChREBP的表达,进一步抑制脂肪酸合成酶的水平,减少脂肪沉积,改善脂肪代谢。[6,7]
04调节胆固醇代谢
下调酰基辅酶A、胆固醇酰基转移酶-2的表达,减少细胞对胆固醇的摄取和细胞的单层通透性。[8]
上调甾醇27-羟化酶、胆固醇-7α-羟化酶的基因表达,抑制肠道对胆固醇的吸收。[9]
通过AMPK途径,降低血浆中低密度脂蛋白胆固醇、游离脂肪酸和总胆固醇水平,并能提高血浆中高密度脂蛋白胆固醇水平。[10,11]
05缓解身体炎症,减少氧化应激损伤
通过抑制激活蛋白1的结合来抑制环氧合酶-2的表达来发挥抗炎作用。[12]
通过复杂的机制如激活AMPK、抑制NF-κB和AP-1通路、调节Nrf2通路等,来改变氧化应激标志物和抗氧化酶的水平,并能减少促炎细胞因子如TNF-α、IL-13、IL-6、IL-8等在机体内的水平。[13]
06调节肠道菌群,改善代谢紊乱
通过改变肠道菌群的结构和群落组成,如抑制有害菌,增加双歧杆菌等有益菌的生长,尤其是能够增加产生短链脂肪酸的菌群数量,从而使肠道菌群更丰富多样。[14]
通过调节微生物-肠道-脑轴改善代谢紊乱。[15]
小檗碱应用中的局限性
尽管小檗碱在血糖代谢和体重体质管理方面受到市场热捧,但是各品牌方陆续发现其在应用上却存在着较大的局限性,如生物利用度低,肠道吸收率差,起效剂量大、造成植物需求量大,生态环境压力大;以及高剂量使用会带来的一些身体不适,如部分人出现过敏反应;高剂量会导致腹痛、腹泻、恶心、胀气、便秘和胃痛等不良反应;有些人甚至会由于高剂量的小檗碱而导致动脉低压、呼吸困难,出现类似流感的症状,以及心脏损伤和胃溃疡等[16]。

造成小檗碱生物利用度低的原因[16]
二氢小檗碱,生物利用度更佳的小檗碱
二氢小檗碱是一种天然存在的生物碱,是小檗碱的一种生物活性形式,在结构与功能上与小檗碱相似。但是,二氢小檗碱具有比小檗碱更高的生物利用度、更强的功效、以及更好的安全性。
二氢小檗碱生物利用度更高的原因是,小檗碱经口服进入肠道后,会在肠道内被还原为二氢小檗碱,经肠壁吸收后再转化为小檗碱进入血液中发挥作用。因此,二氢小檗碱可以更快地被肠壁吸收,因而使其生物利用度比小檗碱高。
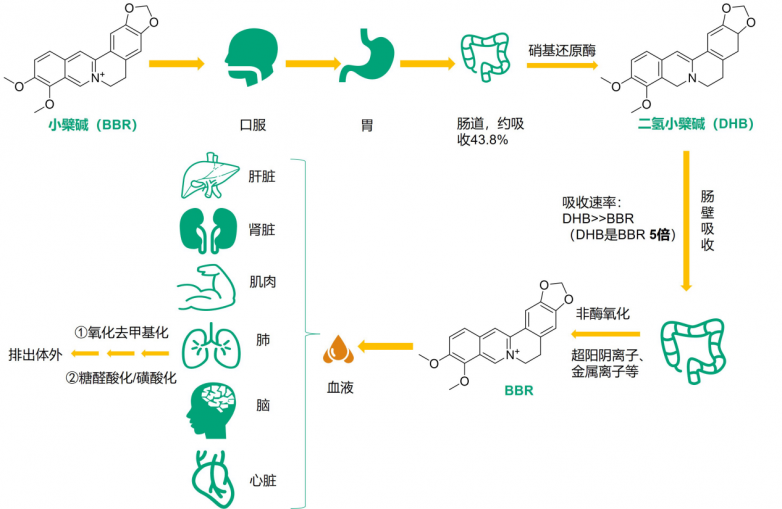
小檗碱在体内的代谢过程[17]
二氢小檗碱,比小檗碱更佳的吸收率
体外吸收:研究表明,以人结肠癌细胞系中的Caco-2细胞为模型,发现二氢小檗碱的吸收速率是小檗碱的11.9倍,外流比率是小檗碱的1/20。[17]
动物体内吸收:研究表明,二氢小檗碱以200mg/kg的剂量灌喂大鼠,在血浆中检测到的二氢小檗碱水平低于10ng/mL,而小檗碱的AUC(0-t)值为261.8nm/mL*h,Cmax为52.47nm/mL,说明二氢小檗碱在肠道内几乎完全转化为小檗碱;而在同时饲喂200mg/kg二氢小檗碱和200mg/kg小檗碱的情况下,二氢小檗碱组的血浆中小檗碱AUC(0-t)值和Cmax分别为小檗碱组的4.8倍和3.25倍,表明二氢小檗碱的肠道吸收更好,更有利于提高血浆中小檗碱的水平。[17]
人体剂量研究:在一项口服100mg、200mg二氢小檗碱和500mg小檗碱的人体实验中发现,100mg和200mg剂量的二氢小檗碱可使体内血浆的小檗碱水平大于500mg小檗碱剂量组。
二氢小檗碱,比小檗碱更好的健康效益
降糖减脂:相较于小檗碱而言,二氢小檗碱可以更有效地减少脂肪量和降低葡萄糖水平,且仅需100mg/kg剂量的二氢小檗碱即可具有与560mg/kg剂量的小檗碱相类似的降糖和减脂效果,甚至更佳。[19]
抗动脉粥样硬化:MMP-9(金属蛋白酶-9)和EMMPRIN(细胞外基质金属蛋白酶诱导剂)在动脉粥样斑块易损性中具有重要作用,而二氢小檗碱相较于小檗碱而言,可显著降低EMMPRIN的表达,有利于改善动脉粥样硬化。[20]
抗溃疡性结肠炎:研究表明,二氢小檗碱可显著减轻由葡聚糖硫 酸钠引起的临床症状与肠道组织损伤。通过促进肠壁保护蛋白MUC的表达,有利于肠道屏障功能恢复,并能阻断TLR4/MyD88/NF-κB信号通路、降低促炎细胞因子水平。在相同剂量下二氢小檗碱对结肠炎的效果更优于小檗碱。[18]
二氢小檗碱安全性数据
急性毒性研究:通过大鼠进行的急性口服毒性试验表明,二氢小檗碱的LD50大于2000mg/kg,这表明二氢小檗碱具有很好的安全性;14天的口服毒性剂量范围试验表明,二氢小檗碱的最大耐受量为120mg/kg;90天的亚慢性毒性试验表明,二氢小檗碱在剂量为100mg/kg时,无不良反应发生[22]
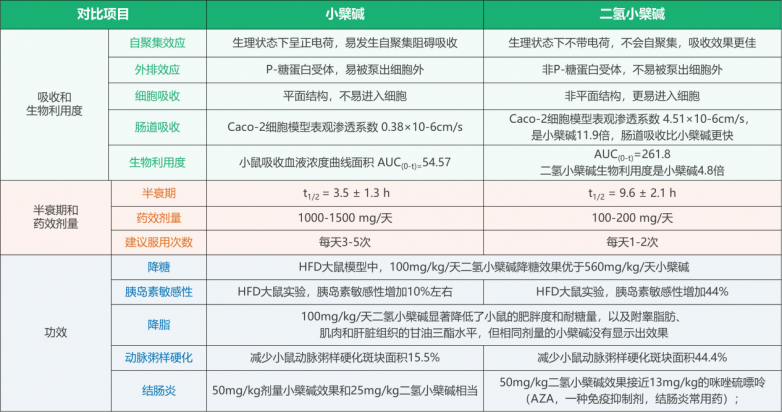
二氢小檗碱与小檗碱的比较(1)

二氢小檗碱与小檗碱的比较(2)
GlucoSober®二氢小檗碱,工艺专利&独特晶型
随着二氢小檗碱在减肥、降糖方面的功效受到持续关注以来,相应的需求与日俱增。二氢小檗碱因为生物活性高,产品抗氧化性强,很容易氧化降解。为解决普通二氢小檗碱见光易降解易结块等应用难题,Bonerge开发了独特晶型的稳定性强高品质的GlucoSober®二氢小檗碱。
本着可持续发展,人与自然和谐发展的经营理念,GlucoSober®通过独家专利的独创生物催化工艺,利用宝贵且日益贫瘠的植物资源,生产出更多高品质的GlucoSober®二氢小檗碱,独特晶型专利工艺。
为了更方便下游片剂和胶囊产品的生产加工,GlucoSober®率先开发了高密度的二氢小檗碱,产品具有更好的流行性,加工过程中减少原料的浪费,更加环保和高效。

高品质原料是制造优质产品的基础,这是Bonerge在参加多个国际论坛与展会后与专家们达成的一个共识。
Bonerge将会持续不断的,一如既往的加大产品研发和循证营养学投入,与全球的合作伙伴一起把GlucoSober®应用到更多健康领域,坚守用爱做产品,让更多消费者因为我们的产品而获得健康效应是我们由衷的喜悦和创新的动力源泉。
参考文献
[1] YU Y, HAO G, ZHANG Q, et al. Berberine induces GLP-1 secretion through activation of bitter taste receptor pathways [J]. Biochem Pharmacol, 2015, 97(2): 173-7.
[2] KONG W J, ZHANG H, SONG D Q, et al. Berberine reduces insulin resistance through protein kinase C-dependent up-regulation of insulin receptor expression [J]. Metabolism, 2009, 58(1): 109-19.
[3] MI J, HE W, LV J, et al. Effect of berberine on the HPA-axis pathway and skeletal muscle GLUT4 in type 2 diabetes mellitus rats [J]. Diabetes Metab Syndr Obes, 2019, 12: 1717-25.
[4] XIA X, YAN J, SHEN Y, et al. Berberine improves glucose metabolism in diabetic rats by inhibition of hepatic gluconeogenesis [J]. PLoS One, 2011, 6(2): e16556.
[5] ZHANG Z, ZHANG H, LI B, et al. Berberine activates thermogenesis in white and brown adipose tissue [J]. Nat Commun, 2014, 5: 5493.
[6] REN G, GUO J H, QIAN Y Z, et al. Berberine Improves Glucose and Lipid Metabolism in HepG2 Cells Through AMPKalpha1 Activation [J]. Front Pharmacol, 2020, 11: 647.
[7] ZHU X, BIAN H, WANG L, et al. Berberine attenuates nonalcoholic hepatic steatosis through the AMPK-SREBP-1c-SCD1 pathway [J]. Free Radic Biol Med, 2019, 141: 192-204.
[8] WANG Y, YI X, GHANAM K, et al. Berberine decreases cholesterol levels in rats through multiple mechanisms, including inhibition of cholesterol absorption [J]. Metabolism, 2014, 63(9): 1167-77.
[9] KONG W, WEI J, ABIDI P, et al. Berberine is a novel cholesterol-lowering drug working through a unique mechanism distinct from statins [J]. Nat Med, 2004, 10(12): 1344-51.
[10] KIM W S, LEE Y S, CHA S H, et al. Berberine improves lipid dysregulation in obesity by controlling central and peripheral AMPK activity [J]. Am J Physiol Endocrinol Metab, 2009, 296(4): E812-9.
[11] JIANG D, WANG D, ZHUANG X, et al. Berberine increases adipose triglyceride lipase in 3T3-L1 adipocytes through the AMPK pathway [J]. Lipids in Health and Disease, 2016, 15(1).
[12] ZOU K, LI Z, ZHANG Y, et al. Advances in the study of berberine and its derivatives: a focus on anti-inflammatory and anti-tumor effects in the digestive system [J]. Acta Pharmacol Sin, 2017, 38(2): 157-67.
[13] LI Z, GENG Y-N, JIANG J-D, et al. Antioxidant and Anti-Inflammatory Activities of Berberine in the Treatment of Diabetes Mellitus [J]. Evidence-Based Complementary and Alternative Medicine, 2014, 2014: 1-12.
[14] ADEL-MEHRABAN M S, AGHABEIGLOOEI Z, ATLASI R, et al. Berberine as a Natural Modifier of Gut Microbiota to Promote Metabolic Status in Animal Studies and Clinical Trials: A Systematic Review [J]. 2023: 202-16.
[15] SUN H, WANG N, CANG Z, et al. Modulation of Microbiota-Gut-Brain Axis by Berberine Resulting in Improved Metabolic Status in High-Fat Diet-Fed Rats [J]. Obes Facts, 2016, 9(6): 365-78.
[16] XU H-Y, LIU C-S, HUANG C-L, et al. Nanoemulsion improves hypoglycemic efficacy of berberine by overcoming its gastrointestinal challenge [J]. Colloids and Surfaces B: Biointerfaces, 2019, 181: 927-34.
[17] FENG R, SHOU J-W, ZHAO Z-X, et al. Transforming berberine into its intestine-absorbable form by the gut microbiota [J]. Scientific Reports, 2015, 5(1).
[18] LI C, DONG N, WU B, et al. Dihydroberberine, an isoquinoline alkaloid, exhibits protective effect against dextran sulfate sodium-induced ulcerative colitis in mice [J]. Phytomedicine, 2021, 90.
[19] TURNER N, LI J Y, GOSBY A, et al. Berberine and its more biologically available derivative, dihydroberberine, inhibit mitochondrial respiratory complex I: a mechanism for the action of berberine to activate AMP-activated protein kinase and improve insulin action [J]. Diabetes, 2008, 57(5): 1414-8.
[20] KIM S, CHUNG J H. Berberine prevents UV-induced MMP-1 and reduction of type I procollagen expression in human dermal fibroblasts [J]. Phytomedicine, 2008, 15(9): 749-53.
[21] BUCHANAN B, MENG Q, POULIN M M, et al. Comparative pharmacokinetics and safety assessment of transdermal berberine and dihydroberberine [J]. PLoS One, 2018, 13(3): e0194979.
[22] LEWIS K D, FALK M. Toxicological assessment of dihydroberberine [J]. Food Chem Toxicol, 2022, 168: 113301.
免责声明:
上述声明均来源于科研文献,未经过国家权威机构评估。本产品不用于诊断、治疗、治愈或预防任何疾病。某些声明可能不适用于所有地区,产品标签和相关声称根据不同政府要求可能会有所不同。解释权归邦尚所有。